
Şalkonlar (kalkonlar), flavonoid bazlı bileşikler olup başta antibakteriyel, antiviral, antikanser, sitotoksik, anti-oksidan, antiülser, anti-hipertansif, anti-diabetik, anti-histaminik, anti-enflamatuar, anti-fungal olmak üzere çok geniş biyoaktif özeliklere sahiptirler.
Ana polifenol ailesi üyelerinin şematik gösterimi aşağıdadır ve polifenoller fenol halkaları baz alınmak suretiyle ve fenol halkalarına bağlanan yapısal sübstitüentlere göre; fenolik asitler, flavonoidler, stilbenler ve lignanlar olmak üzere 4 ana gruba ayrımlanabilmektedirler.
Flavonoidler ise başlıca şalkonlar, flavonoller, flavonlar, flavanonlar, antosiyanisidinler, ve izoflavonoidler olarak ayrımlanmaktadır. Çekirdek 1,3-difenil-2-propenon şalkon yapısı da şemadaki gibidir (Şekil 1).
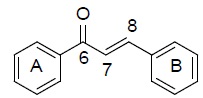
Şalkonlar, flavonoid ailesi üyesi olup, doğal ya da sentetik olarak mevcut olabilen bileşiklerdir ve geniş bir biyolojik aktivite spektrumuna sahiptirler. Antibakteriyel, antiviral, antikanser, sitotoksik, anti-oksidan, antiülser, anthelminitik, anti-hipertansif, anti-diabetik, anti-retroviral, anti-histaminik, anti-enflamatuar, amoebicidal, anti-tüberküloz, anti-fungal, antiprotozoal, ve böcek öldürücü etkileri rapor edilmiştir (Şekil 2). Şalkonlar, kimyasal olarak üç karbonlu bir α, β doymamış karbonil sistemiyle birbirine bağlanan iki aromatik halkadan (1,3-diaril-2-propen-1-on iskeleti) meydana gelirler.
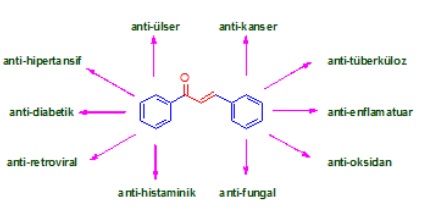
Günümüze kadar çok sayıda kalkon türevi literatüre girmiş olsa da, bu bileşiklerin sahip oldukları geniş biyolojik özellikleri göz önüne alındığında yeni şalkon türevlerinin sentezlenmesine hala gereksinim söz konusudur.
Şalkonlar, heterosiklik C halkası eksik olan flavonoidlerdir, biyolojik aktiviteleri de yüksektir. En önemli şalkon tipi bileşikler; floretin, floretin türevleri, floretin glukozid floridzin (floretin 2’-O-glukoz), arbutin, ve şalkonaringenin olmaktadır (Şekil 3).
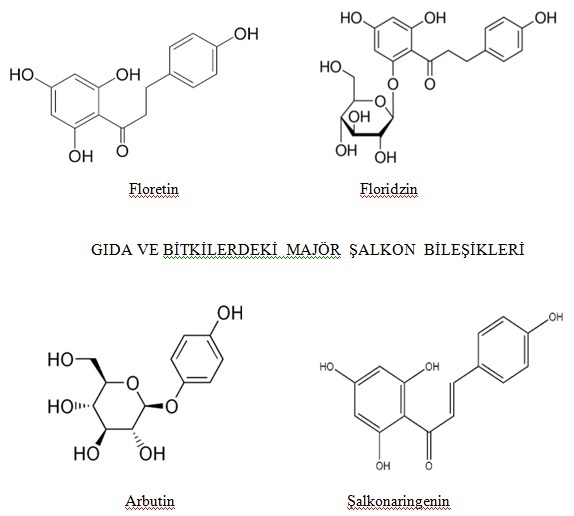
Floretin ve floridzin, elmanın karakteristik bileşikleridir. Şalkonaringenin domateslerin karakteristik bileşiği olmaktadır. Arbutin, armutların karakteristik fenolik bileşenidir; çileklerde ve ayı üzümünde de önemli düzeydedir. Arbutin ayrıca buğday ve buğday ürünlerinde mevcuttur ve eser düzeyde de çay, kahve, kırmızı şarap ve brokolide bulunmaktadır (Şekil 4). Başlıca Şalkon Kaynağı Bitkiler ise ashitaba, okaliptüs ve Meyanköküdür ev bunların çaylarıdır (Şekil 5).


Gıda kaynaklarından şalkonların biyoyararlılığı üzerine çalışmalar sınırlıdır ancak sentetik şalkonlar, biyolojik özellikleri çalışılmak suretiyle geniş ölçüde rapor edilmiştir.
Şalkonların Antikanser Özelliği
Şalkonlar, hücre döngülerinin inhibitörleri olmaktadırlar. Şalkon ve şalkon türevlerinin antiproliferatif aktivitesi, kanser hücre döngüsünü tutuklaması ve hücresel apoptotik makineleşmeyi başlatması ile çok yakından ilişkilidir.
Siklinler ve siklin bağımlı kinazlar (Cdks),iki önemli düzenleyici faktördür ve hücre döngüsü ilerlemesinde önemli bileşenlerdir. Bu bileşiklerin ekspresyon ya da transkripsiyon sonrası modifikasyonlarına yönelik değişiklikler, hücre döngüsü fonksiyonlarının deregülasyonuna yol açar
Şalkonların, hücresel proliferasyon, angiogenesis, metastaz, apoptosis ve multidrug resistansının iptali ile ilişkili sinyal transdüksiyon metabolik yollarının birçok noktasına müdahale ettiği rapor edilmiştir ve şalkonlar antikanser etkiye sahiptirler ve antirezistans etkilidirler (Şekil 6).
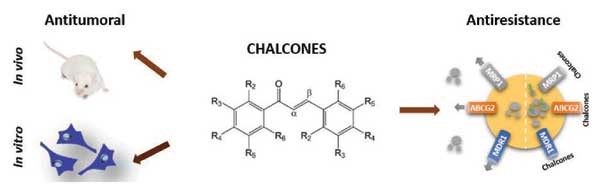
Şalkonlar, hücre döngüsü ilerlemesi ile interaksiyona girmekte olan potansiyal ajanlardır. Şalkon ajanları etkisiyle, siklin B1, siklin A, ve Cdc2 düzeylerinin indirgenmesi ve p21 ve p27 ekspressiyonlarının zenginleşmesinin bir arada olması, hem insan MCF-7 ve MDA-MB-231 meme kanseri hücre hatlarındaki hem insan T24 ve HT-1376 mesane kanseri hücre hatlarındaki G2/M fazının tutuklanmasına yol açabilmektedir ve şalkonların ilgili CA hücre hatlarının inhibisyonu üzerinde çok etkili oldukları rapor edilmiştir.
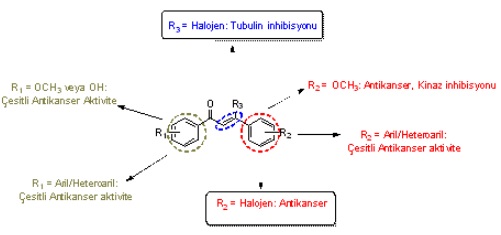
Şalkonların antikanser özellikleri özellikle iki aromatik halkadaki fonksiyonel grup çeşitliliğinden etkilenmektedir. Anti-kanser etki gösteren şalkonların yapısal özellikleri incelendiğinde, ABCG2/Pgp/BCRP, 5α-redüktaz, aromataz, 17-β-hidroksisteroid dehidrogenaz, HDAC/Situin-1, VEGF, VEGFR-2 kinaz, MMP-2/9, CDC25B, tubulin, katepsin-K, topoizomerazII, Wnt, NF-kB, B-Raf ve mTOR gibi çeşitli moleküler hedefleri inhibe ettiği bildirilmektedir.
Şalkonların Sentezleri
Şalkonlar, polar bir solvent (metanol vb) eşliğinde kolaylıkla bir aldehid ve uygun bir ketonun baz katalizli Claisen-Schmidth kondensasyonu ile sentez edilebilmektedir. Metod, çok yönlü ve pratiktir, ürünler değişken olabilmektedir.
Şalkonlar üzerinde yapılan yapı-aktivite çalışmaları, aril halkaları üzerinde elektron sağlayıcı/ elektron çekici gruplarile yapılan sübstitüsyon veya şalkon yapısına aril/heteroaril gruplarının takılmasının antikanser aktivite üzerinde çok önemli bir etki sağladığını göstermektedir. Günümüze kadar yapılan çalışmalar, potansiyel ilaç adayı olan kalkon bileşiklerinin flor sübstitüe türevlerinin ve flor atomu ihtiva edenş-hibrit bileşiklerinin test edilen değişik kanser hücrelerinde aktivite üzerinde pozitif anlamda bir katkı sağladığını göstermektedir (Şekil 7).
KAYNAKÇA
Orlikova B., Tasdemir D., Golais F., Dicato M., Diederich M. 2011. Dietary chalcones with chemopreventive and chemotherapeutic potential. Genes Nutr. 6,125–147
Burnmaoğlu S. 2017. Anti-Kanser Aktiviteye Sahip Bileşikler Olarak Flor-Sübstitüe Kalkonlar. K. Fen Müh. Derg. 7(2), 658-664.
Hsu YL, Kuo PL, Tzeng WS, Lin CC . 2006. Chalcone inhibits the proliferation of human breast cancer cell by blocking cell cycle progression and inducing apoptosis. Food Chem Toxicol 44, 704–713.
Shen KH, Chang JK, Hsu YL, Kuo PL 2007. Chalcone arrests cell cycle progression and induces apoptosis through induction of mitochondrial pathway and inhibition of nuclear factor kappa B signalling in human bladder cancer cells. Basic Clin Pharmacol Toxicol 101, 254-261.
Tokuşoğlu Ö. 2018. Antikarsinojen ve Antiproliferatif Ajanlar. Gıda Biyoaktifleri Lisansüstü Ders Notları (İZİNSİZ KOPYALANAMAZ, ÇOĞALTILAMAZ. HER HAKKI MAHFUZDUR).

